一、使用共识标准对FDA审评为何很重要?
FDA自愿共识标准,对医疗器械从业者和FDA工作人员无疑是宝贵资源。几十年来,FDA一直支持并依赖共识标准的制定和使用,以支持FDA保护和促进公共卫生的使命。
共识标准为医疗器械安全性和有效性评估的特定方面提供了共识方法,如:试验方法、验收标准、风险管理和可用性等领域的处理流程。
适当使用共识标准,能提高可预测性,简化上市前审评,得到更明确的监管预期,促进国际协调,可有效证明上市前过程中安全性、有效性或实质等同性的各方面,减少申请人所需提供的文件量,可缩短FDA审评时间,从而加快安全有效的医疗产品进入市场。
二、FDA共识标准是如何识别和选取的?
通常,国内医疗器械产品如需获得美国FDA批准进入美国市场,首先应证明器械安全性和有效性,而最有效直观的方法就是提交器械需满足的各类测试报告(性能测试/生物相容性测试/有源产品电气安全/EMC测试等)。但相较欧盟和国内,FDA对测试标准选取有其自身要求:相关测试需执行FDA认可共识标准(由私营部门标准组织以共识程序制定)。
FDA认可的共识标准(全称Recognized Consensus Standards)是经FDA评估和认可的用于满足监管要求,且FDA已在联邦公报发布通告的共识标准。
换言之便是FDA在对行业内高频使用的各类标准进行识别评估后,选择合适的标准并形成FDA官方所认可的标准体系。例如:FDA采用ISO、ASTM、ANSI AAMI ISO、USP-NF等组织发布的一系列标准,作为生物相容性认可的共识标准。
FDA官网中可查询到最新认可的共识标准,制造商可根据自身产品实际情况,结合未来需要销售的区域,选择共识标准库中合适的标准进行产品的验证。
三、怎样快速准确查到FDA共识标准?
1. FDA共识标准数据库链接
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfStandards/search.cfm
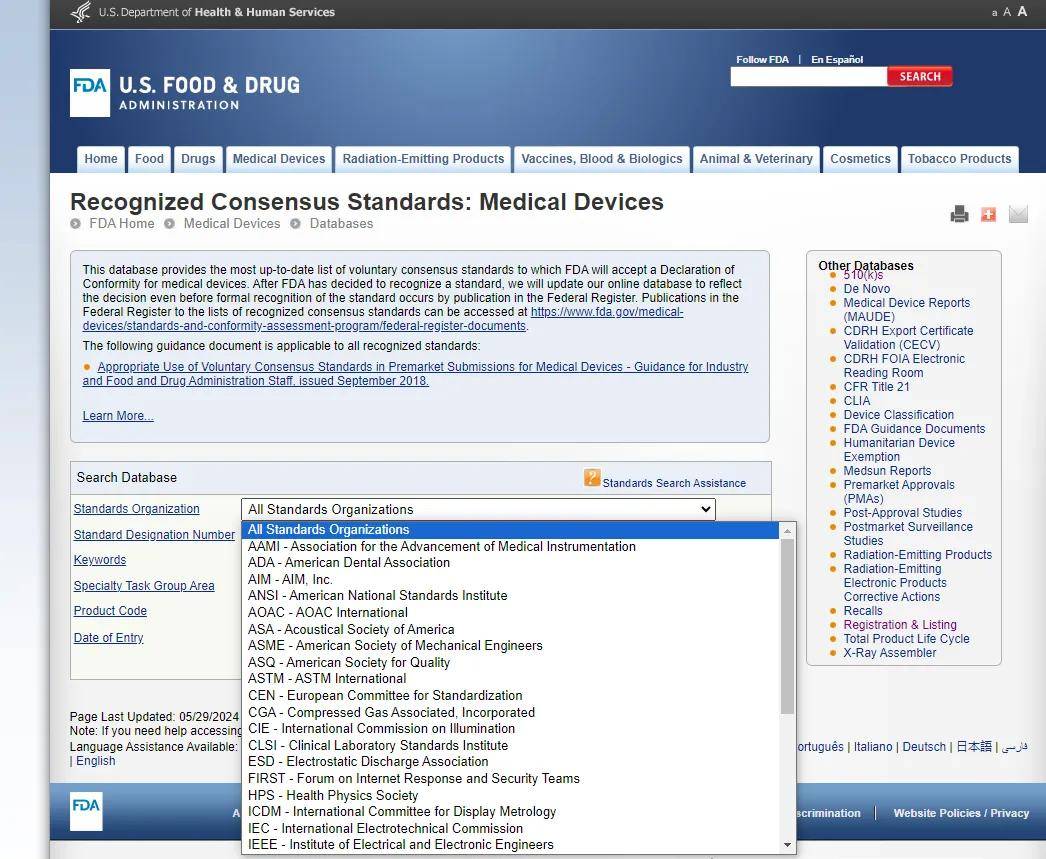
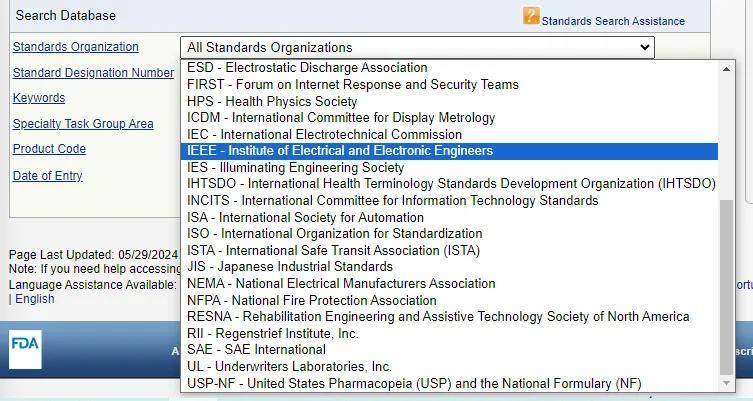
由图可知共识标准来源广泛,除ISO还有IEC,CEN,JIS等系列标准,国内执行的国标尚未列入共识标准体系,因而不属于FDA认可的共识标准。
制造商在进入美国市场前,建议根据目标销售区域选取ISO,IEC,ASTM,AAMI等标准对产品进行检测。
2. 查询方式
「 方式1 」

在上图中红框处输入标准号 (只输入数字),再点击Search。
「 方式2 」
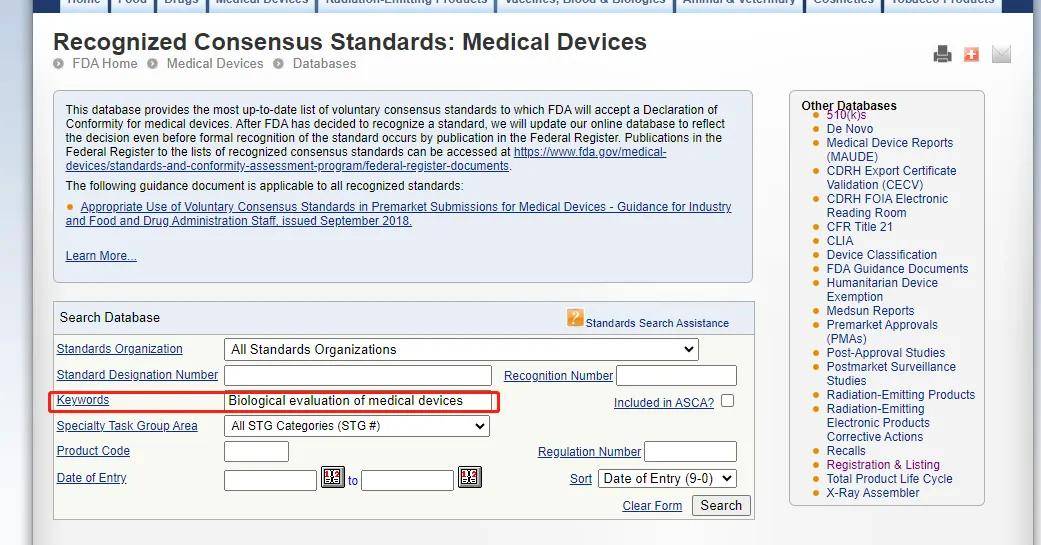
在关键字一栏输入标准名称或标准关键字信息,再点击search。得到以下查询页面↓
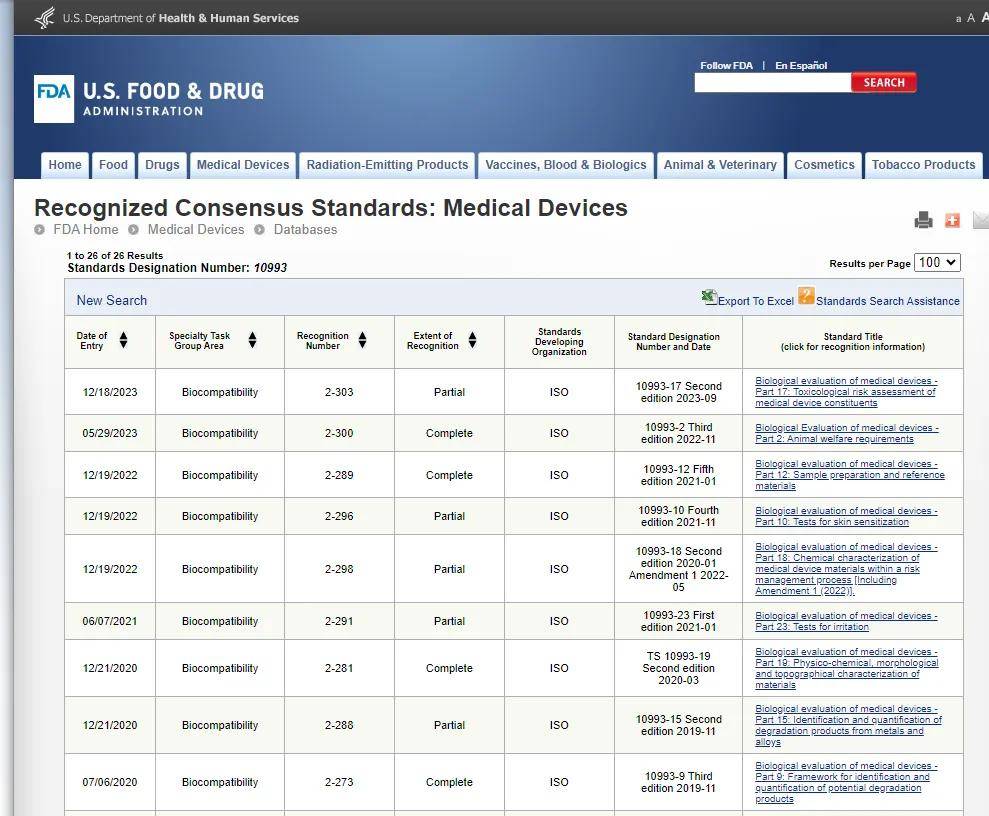
从以上页面中清晰可见:共识标准库内FDA最新的10993(生物相容性)标准的共识情况,每个被纳入共识标准库中的标准均配有编号即共识标准号,另有当前标准版本号、共识标准库内的专业分类情况等系列信息。
# FDA 510(k)申请好帮手,非久顺莫属!#
[久顺企管集团]近30年全球合规技术专家&资深美代,成员超80%本科\硕士\博士,丰富海外留学经验,无障碍英语口语\书面交流,一站式高效率FDA合规服务: 上市前批准(510k\特殊510k\豁免510k);申请创建UDI-DI\GUDID账户;QSR820体系建立维护;性能研究方案编写;临床性能方案制定;临床试验实施;FDA验厂等。