1.使用适应症Indications for Use的概念与作用
医疗器械认证申报开始前,我们应明确产品具体分类。无论是产品计划往美国还是往欧洲上市,分类都将决定器械的监管途径、器械受到的相应审查级别。
监管机构会考虑诸多因素用于确定器械分类,特别是预期用途\目的因素。而其中,使用适应症(即:谁、何时、何地、如何使用器械)发挥着举足轻重的作用与影响力,并且还时常被误解。事实上,器械使用适应症中寥寥数语的细微变动,便能明显改变器械的监管路径。
2.预期用途VS使用适应症的区别
预期用途:
描述器械的整体功能和用途,但未具体说明医疗条件或患者群体。预期用途声明通常是对器械及其功能的简洁、高级描述。
使用适应症:
提供器械应用于医疗条件、疾病或情况的具体细节,其缩小器械适用范围,并确定目标人群或特定患者特征。使用说明书中的适应症声明应得到临床数据的支持。
需注意:切勿混淆使用适应症和预期用途。
举例说明↓预期用途和使用适应症的差异:
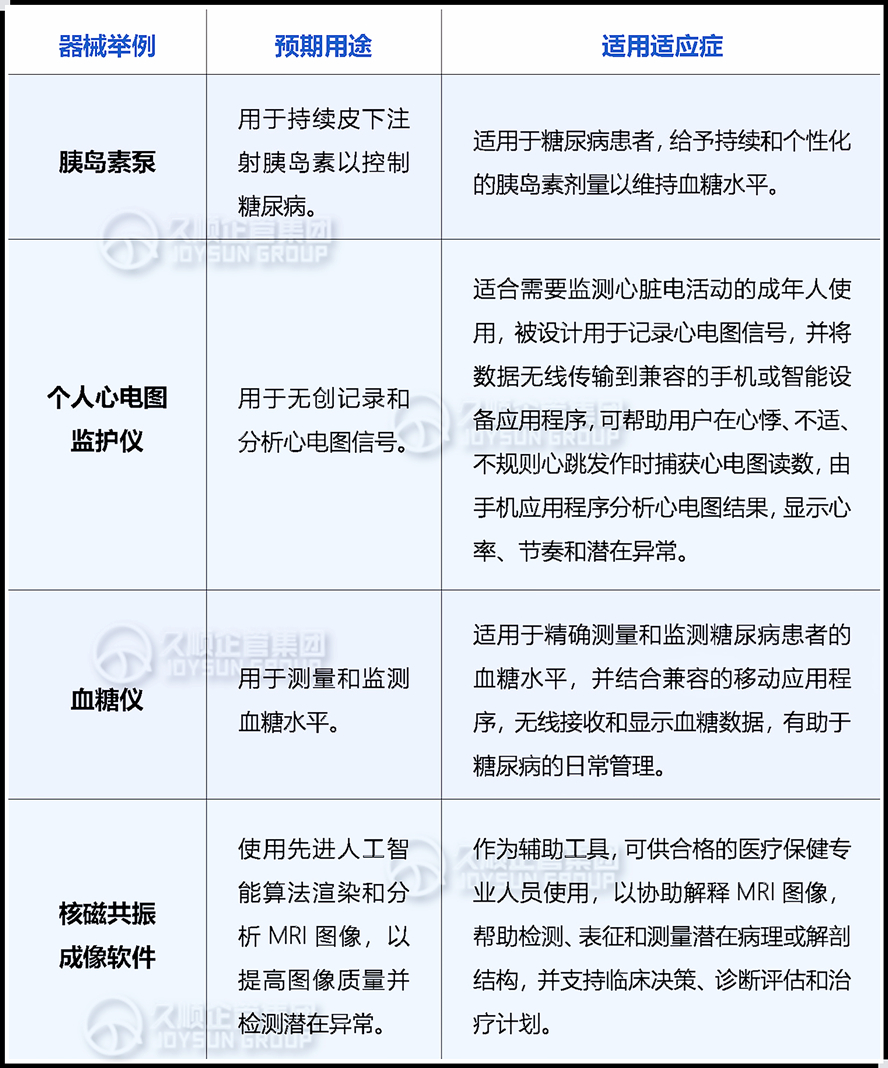
3.使用适应症对FDA医械分类的影响
美国FDA实施三级分类等级,对应从低至高的器械风险和更趋严格的监管要求:
Class I低风险 >> Class II中风险 >> III类高风险
低风险、新型或高风险器械除外,大部分II类器械需要向FDA提交上市前通知510(k)。 510(k)是关于器械的文件档案,证明器械基本等同于FDA已批准器械(对比器械),已批准器械被分配3个字母构成的器械代码,FDA使用该代码以识别和跟踪相似器械类型。
器械的使用适应症必须与对比器械的使用适应症及器械代码一致,改变或缩减使用适应症可能改变对比器械和器械代码。
例如:假设计划将某种组织粘合剂推向市场。如果粘合剂用于局部微创手术切口,则可能是II类器械。如果粘合剂用于内部或眼科,则可能是III类设备,甚至可能需要上市前授权(PMA)。此外,如果粘合剂用于内部或眼科,将有一个不同的器械代码。当使用适应症被扩大时,监管可能变得更加严格,特别是如果使用适应症指向身体部位或治疗方案时,则此时使用适应症本质上具备更高的风险。
4.使用适应症对欧盟医械分类的影响
与FDA类似,根据欧盟医疗器械法规MDR2017/745,器械风险等级由低至高划分为:
I类 >> IIa类 >> IIb类 >> III类
欧盟的器械分类与对比器械无关,其分类系统完全基于规则。如果多个规则适用于器械,则依据最高风险关联的规则确定其分类。例如:短期使用的侵入性器械为IIa类,与心脏直接接触则为III类。
欧盟体外诊断医疗器械法规IVDR 2017/746执行类似系统,该系统包括7条规则和4层分类(A类>B类>C类>D类)。
欧盟分类规则从预期用途的3个主要类别开始:器械是非侵入性,侵入性,还是有源?
在此基础上,按照规则逻辑确定器械分类。器械使用适应症则进一步告知适用于器械的规则。
上文举例的粘合剂器械的分类含义在欧盟是相似的。外用粘合剂可视为非侵入性IIb类器械;然而,内部粘合剂尤其是与心脏接触的粘合剂,可能是侵入性III类器械。
>> FDA与CE申请,欢迎感受久顺速度!【久顺企管集团】近30年全球合规技术专家、资深欧代+美代,荷兰、英国、美国、中国均设公司,超80%本科、硕士、博士比例+海外留学经验,无障碍英语口语和书面交流。
· 美国合规服务:FDA法规符合性咨询及培训、证书获取、QSR820体系建立维护、验厂、510(K)\Pre-submission\De Novo分类请求的文件编制\递交\进度跟踪等。
· 欧盟合规服务:辅导升级体系以符合MDR\IVDR法规,帮助短时间内建立运行质量管理体系,编写技术文档,辅导通过公告机构审核,快捷获取CE证书。









 沪公网安备 31011502005499
沪公网安备 31011502005499