一、FDA2024财年起始,开启付费模式!
按照FDA规定,每年10月1日至12月31日为下一年度再注册的时间,也意味着:发文时间距离2023财年结束仅剩2周不到的时间!
而FDA的2024财年 (2023年10月1日至2024年9月30日)用户费用已发布如下↓
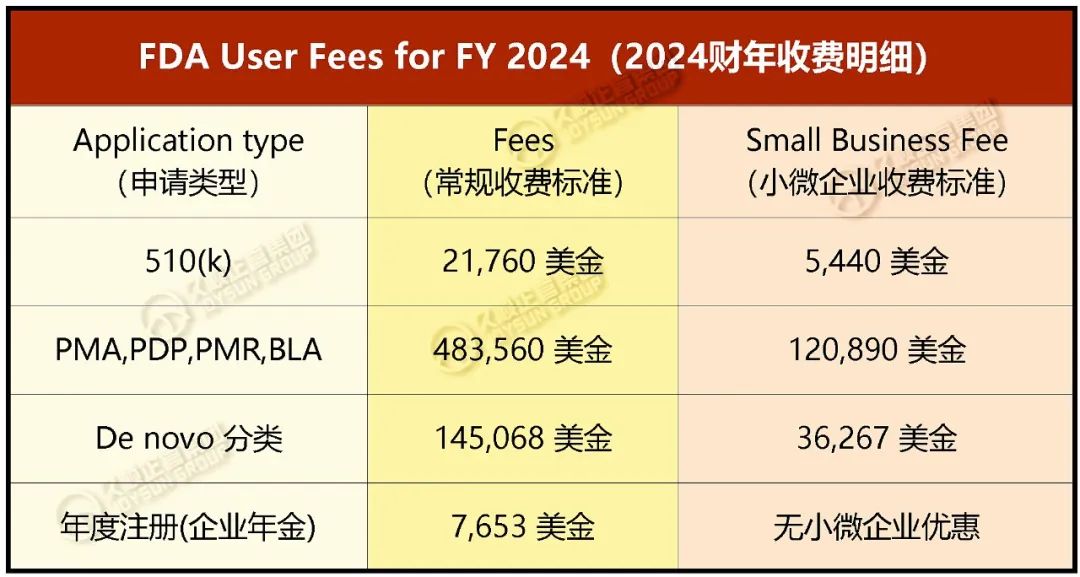
对比2023财年,2024财年用户费用上浮9.5%,年度注册费涨幅达17.87%。
为您盘点近5年510(k)收费变化趋势↓
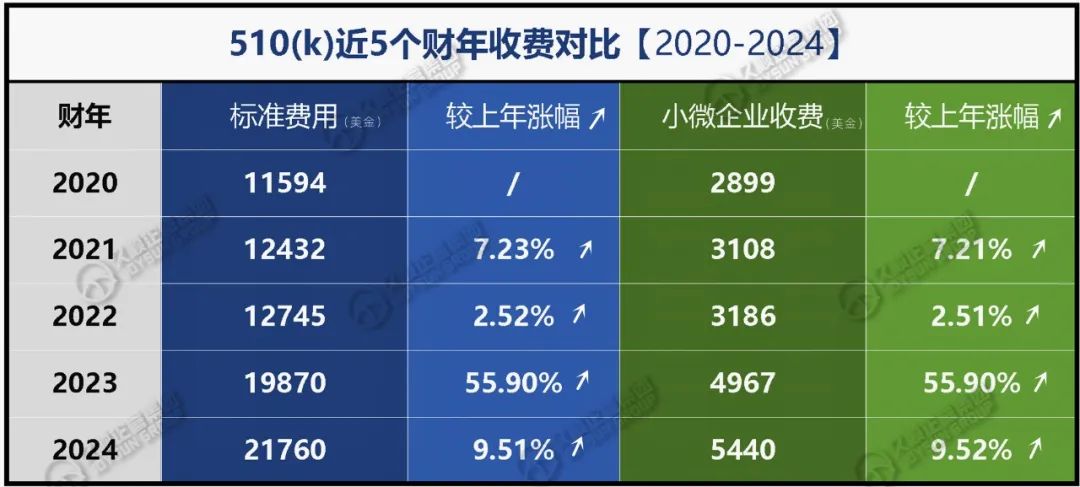
* 重要提示 *
1.如果企业未支付费用,FDA就无法启动审查所提交的申请,包括:510(k)、PMA、De Novo提交的材料。
2. FDA为提交指定审查人员前,企业必须全额支付相应器械申请费(但豁免除外),而小微企业则有资格享受更低价格的收费。
3.2023财政年度的510K提交,必须在美国东部时间29日16点前上传至客户协作门户网站CCP或由文件控制中心DCC通过快递接收。
4.FDA年费的支付,企业通过美元账户转账时应在转账单上注明年金的PIN号,如未注明,汇款有遗失风险。
5.企业未完成FDA年度注册, FDA系统的许多注册变更则无法开展,企业已完成的豁免510K注册和510K注册将失效,FDA官网将对企业除名。企业如后续希望保持正常出口美国的业务,应提前完成缴纳年费、更新年度注册,并且委托专业机构进行操作。
6.企业申请FDA注册必须先完成邓白氏编码(DUNS)申请(邓白氏编码是美国境外企业在FDA注册时,FDA官方要求必须提供的企业信息之一)
不必麻烦!如果您有邓白氏编码的注册需求,可联系具有丰富成功案例的久顺。
二、2023财年小微企业资质,进入失效模式!
首先应明确概念:小微企业申请表上的“FY2023”所代表的不是自然年,而是FDA的财政年度即“2022年10月1日至2023年9月30日”。
* 重要提示 *
1.如果企业已获得2023财年小微企业号,则有效期至2023年9月30日结束,从2023年10月1日零点开始,该小微企业申请号将失效。企业如仍需享受小微企业待遇,则应当重新申请。
根据笔者的小微企业辅导经验,第四季度(10-12月)为申请高峰,届时申请周期将会拉长,FDA收到资料受理后会在60天内审查文件并回复。
2.应重点关注:资质申报表格的英文件需企业所在地税务局盖章,否则将无法成功申请。
不必担心!久顺可提供一站式全程化小微企业申请服务,直接对接FDA有关部门免除繁琐流程,提供线上申请和线下递交服务,为企业省去诸多中间环节,助力企业客户2-3周内完成小微企业申请(曾创造3天内成功拿下小微企业号的惊人速度)。
三、510(k)申请递交方式,开始强制模式!
2023年10月1日起,除豁免外,所有510(k)申请必须使用eSTAR在线递交。
eSTAR更加注重实验/检测过程,申请人应对此进行更详细的描述。
首次申请510(K)为2023年10月1日前受理,后续发补资料递交可继续沿用eCopy递交方式!
* 重要提示 *
除满足eSTAR电子递交模板架构信息,所有递交过程中的小细节都不容被忽视:
1.文件大小:eSTAR的 PDF文件若超过1GB则申请处理可能被延迟;确保eSTAR所附图片和视频采用与Windows操作系统相兼容的格式如JPEG、AVC MP4、HEVC MP4。FDA强烈建议使用HEVC进行视频压缩。
2.文件数量:若可行,合并内容相似的附件,以便在eSTAR的每个附件类型问题上只需提供一个附件。FDA建议合并后的文件有书签或目录。
3.现行eSTAR版本:分为体外诊断eSTAR版本1和非体外诊断eSTAR版本2,务必进行正确选择。
4.指导文件&附件文件:eSTAR不需要遵守eCopy指导文件,也不需要被压缩并放在MISC FILES文件夹中;但任何与eSTAR PDF一起提供的附加文件需要符合eCopy指导文件的规定。FDA强烈建议不要在eSTAR PDF中提供附加文件。
5.申请人无需在eSTAR中提供适应证说明页(FDA Form 3881)、上市前审查递交封面页(FDA Form 3514)或符合性声明(如果适用),因为前述都是eSTAR PDF中的内容。此外,如果申请人选择使用eSTAR创建510(k)摘要,则无需在eSTAR中提供额外的510(k)摘要。
不必发愁!久顺已为多家企业完成eSTAR方式的510(k)申请。









 沪公网安备 31011502005499
沪公网安备 31011502005499