近期,为支持监测欧盟市场医疗器械可用性的研究,欧盟公布第12次MDR/IVDR认证和申请的公告机构调查报告。
该调查显示:NB公告机构审核认证效率正日益提升,相应的制造商提交申请数量持续上升可见医疗器械市场对CE证书的大量需求。以下解读的数据统计自:公告机构获得资质授权之日起至2024年10月止。
·MDR申请提交、证书签发数据的统计分析
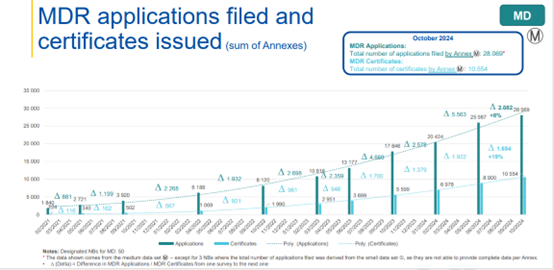
解读1:MDR申请总数为28069,共签发证书数量为10554,相较2024年6月数据,申请数提升2082,涨幅8%;发证数量上升1654,涨幅19%。
从总体观察可见,MDR申请提交数与证书签发数双双呈逐月上升的趋势。
解读2:62%比例为主的情形下,申请递交到正式签约之间耗时为2个月以内。
解读3:占比52%的公告机构中,生产企业获得MDR质量管理体系证书的平均耗时为13-18个月;占比31%的公告机构中,生产企业获得MDR质量管理体系证书的平均耗时为6-12个月。
占比56%的公告机构中,生产企业获得“MDR质量管理体系证书+产品证书”的平均耗时为13-18个月;占比25%的公告机构中,生产企业获得“MDR质量管理体系证书+产品证书”的平均耗时为19-24个月。
解读4:生产企业MDR申请被公告拒绝的原因,最高为54%比例的“非公告机构获授权指定的范畴”,第二为23%比例的“其他因素”,可喜的是此前研究报告发现的“申请有欠缺”的问题有所改进。
针对占比最高被拒原因,厂商应注意在选择公告机构时识别其具体的授权指定的认证审核范围。
·IVDR申请提交、证书签发数据的统计分析
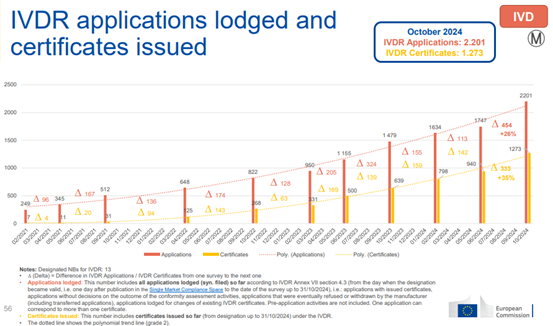
解读5:IVDR申请提交总数2201,证书签发总数1273,相较2024年6月数据,IVDR申请提交总数上升454,涨幅26%;IVDR发证总数上升333,涨幅35%。
从总体观察可见,IVDR申请提交数与证书签发数双双呈现显著上升趋势。
解读6:D类申请提交总数658,证书签发总数377,相较2024年6月数据,D类申请提交总数上升73,发证总数上升107。
解读7: 占比40%的公告机构中,生产企业获得IVDR质量管理体系证书的平均耗时为6-12个月;占比40%的公告机构中,生产企业获得IVDR质量管理体系证书的平均耗时为13-18个月。
占比70%的公告机构中,生产企业获得“IVDR质量管理体系证书+产品证书”的平均耗时为13-18个月;占比10%的公告机构中,生产企业获得“IVDR质量管理体系证书+产品证书”的平均耗时为19-24个月。
从总体而言,绝大部分约80%的公告机构平均用时均高于13个月。
解读8:IVDR申请递交被拒的原因中,最高为57%比例的“其他因素”,第二为“产品资质与分类有误”。
解读9:“申请递交资料的欠缺不充分”问题仍旧未被改进,大部分公告机构意见为申请递交材料完整程度低于50%。
→ 欧盟CE拿证,认证久顺准没错!
√选择久顺就是选择成功!始创于1996年,西班牙\荷兰\英国\美国\中国均设公司,近30年全球合规技术专家。提供全程高效的欧盟合规服务:√CE注册取证√技术文档编写 √合规策略 √体系辅导 √上市后监督咨询 √近20年资深欧代 √编撰临床方案设计\临床试验方案 √收集\整理\分析试验原始数据并出具临床试验报告等。
久顺部分CE成功案例(篇幅有限,仅展示部分)↓
☑辅导优思达生物取得核酸检测领域首批CE-IVDR证书、获国内核酸检测首张IVDR荷兰CIBG注册证书;
☑辅导江苏宏微特斯的HCG早早孕自测试剂盒取得BSI签发B类CE-IVDR证书;
☑辅导全球医械巨头获IIb类产品CE-MDR证书;
☑辅导斯瑞奇获I类灭菌创口贴CE-MDR证书;
☑助力海翔药业取得I类灭菌CE-MDR证书;
☑助力台衡精密测控获I类测量CE-MDR证书;
☑辅导亚美斯特(天津)获得IIa类通气类产品的CE-MDR证书;
☑辅导杭州某生物企业成功通过I类灭菌采样拭子的MDR体系审核(ISO13485);
☑助力深圳客户顺利通过IIa类敷料类产品的MDR体系审核(ISO13485);
☑辅导某跨国医疗器械企业取得IIb类监护类产品CE-MDR证书
☑辅导老客户IIa类手术器械获得莱茵签发的CE-MDR证书...








 沪公网安备 31011502005499
沪公网安备 31011502005499