挪威DNV,斩获IVDR审核资质!
第17家欧盟IVDR审核公告机构诞生:DNV Product Assurance AS (公告机构号:2460) ,是挪威首家IVDR公告机构,成为MDR&IVDR双资质NB机构。
至此,17家IVDR公告机构所属国家分布为:德国4家;荷兰2家;意大利2家;芬兰2家;西班牙1家;比利时1家;爱尔兰1家;法国1家;斯洛伐克1家;奥地利1家;挪威1家。
17家IVDR公告机构完整名单↓
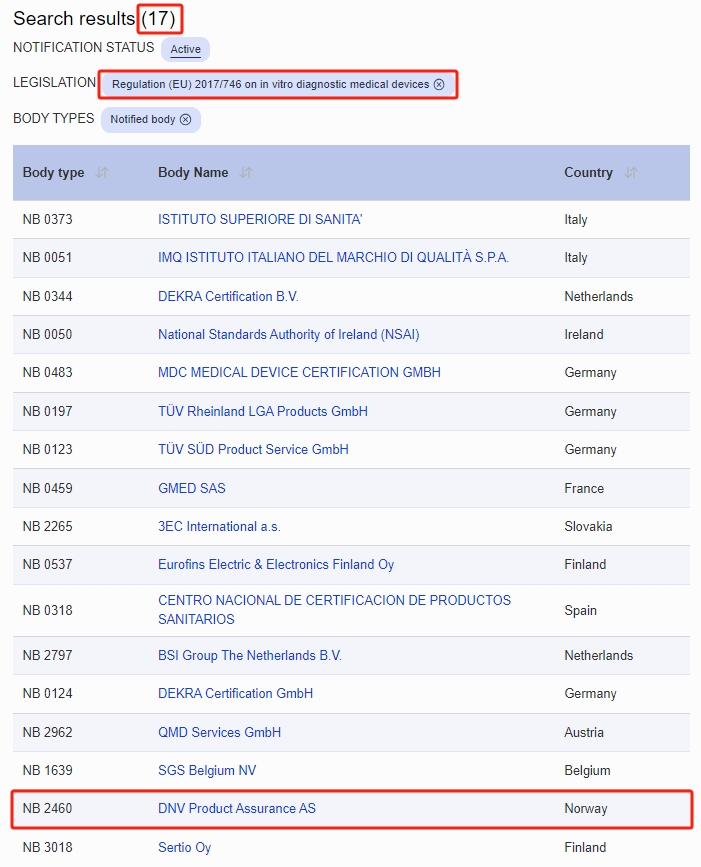
审核资源持续补强~IVDR拿证利好不断!
近年来国内诸多IVD巨头企业均已宣告斩获欧盟CE IVDR证书,由此成功叩开欧盟市场大门,迈向欧洲这一IVD出海关键目的地,不仅奠定获证企业进军欧洲的先发竞争优势,更加速其产品销售进程。
曾经存在的欧盟公告机构承接能力不足痼疾,正日益得到改善,此次IVDR公告机构连续扩充新力量,为制造商IVDR/MDR申请增加新选择、创造有利条件,公告机构数量不足状况将得到持续改善。
#IVDR拿证作用大但难度也不小,选择靠谱的合规服务企业是关键!
→ 欧盟体外诊断CE获证服务,久顺只用案例和实力说话!
√久顺企管已成功辅导优思达获TÜV南德签发IVDR CE证书(10项产品),助力取得国内核酸检测首张IVDR荷兰CIBG注册证书。久顺为优思达提供了精湛的13485体系+IVDR辅导(CE技术文档辅导)、欧代等关键性合规服务。
√久顺也已成功辅导江苏宏微特斯获得BSI签发的HCG早早孕自测试剂盒B类IVDR CE证书,通过差异性分析攻克欧盟临床难题,为客户顺利完成ISO13485结合IVDR法规适用条款的升级,并配合企业成功通过现场审核,仅9个月便超前通过IVDR CE审核。
》作为国内少有的配备IVDR法规\技术\数据分析领域专业团队的企业,久顺已与欧盟各主流实验室和医院建立合作,可提供临床性能研究(国内少有可胜任且使用EP文件研究)、可用性研究、上市后临床跟踪研究等高质高效服务。








 沪公网安备 31011502005499
沪公网安备 31011502005499