新闻法规
飞检暴雷!16家械企质量体系不合规被通报,这些高发问题企业应自查
[2025-08-20]
按照国家药品监督管理局2025年医疗器械检查工作部署,食品药品审核查验中心组织开展了医疗器械生产企业飞行检查工作,发现16家企业质量管理体系存在不符合《医疗器械生产质量管理规范》及附录相关问题,于近日发布第二批通告。
根据本次通告的统计显示: 文件管理(14次,占比11.2%)、采购(12次,占比9.6%)、设计开发(11次,占比8.8%)成为飞检问题重灾区,其中“设计开发“继2025第一批飞检通告上榜后再次进入问题数前3。统计详情见下图↘
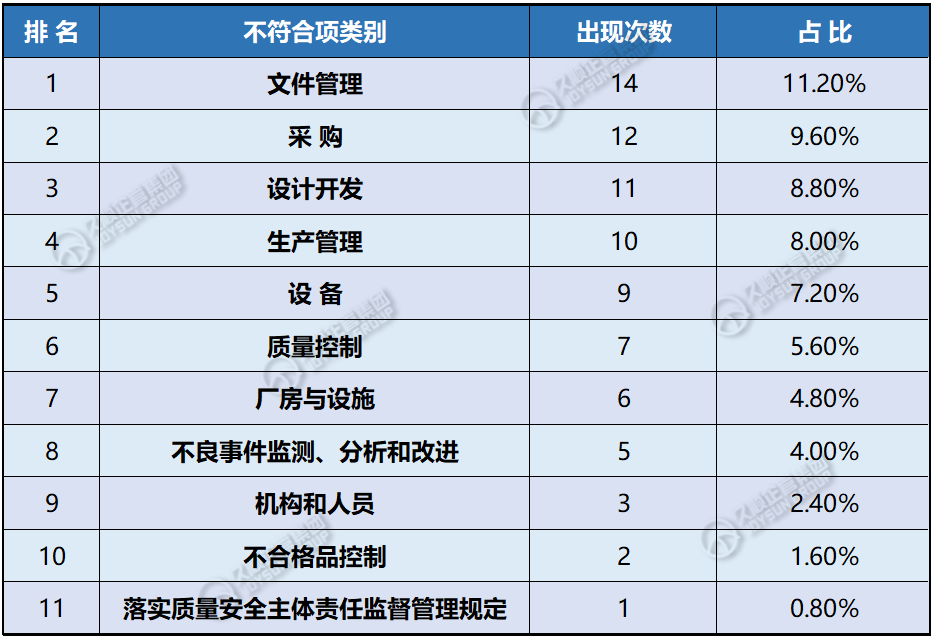
2025年第二批医疗器械飞行检查情况汇总:

来源:国家药品监督管理局食品药品审核查验中心
声明:文章为转载,其版权归原作者所有。转载仅用于分享,若涉及文章版权等问题,联系我方删除!
篇幅有限仅展示部分内容,欲知完整版请关注微信公众号"久顺集团技术服务"(识别或扫描下方二维码即可关注)后查阅对应推文。

#国内注册要快&还要好?认准久顺就对了!
>>【久顺企管集团】医械注册的加速引擎!近30年全球合规技术专家,中国\西班牙\荷兰\美国\英国均设公司,擅长产品注册全程辅导、技术文档编写、质量体系建立完善及咨询等服务,以及CE/FDA/UKCA/CFS等证书办理,具备优厚的咨询管理和技术服务经验及能力,护航产品全球范围高速畅行。
【返回】







 沪公网安备 31011502005499
沪公网安备 31011502005499