按照《医疗器械监督管理条例》《医疗器械分类目录动态调整工作程序》有关要求,结合医疗器械产业发展和监管工作实际,经研究,国家药监局决定对《医疗器械分类目录》部分内容进行调整。现将有关事项公告如下:
一、调整内容
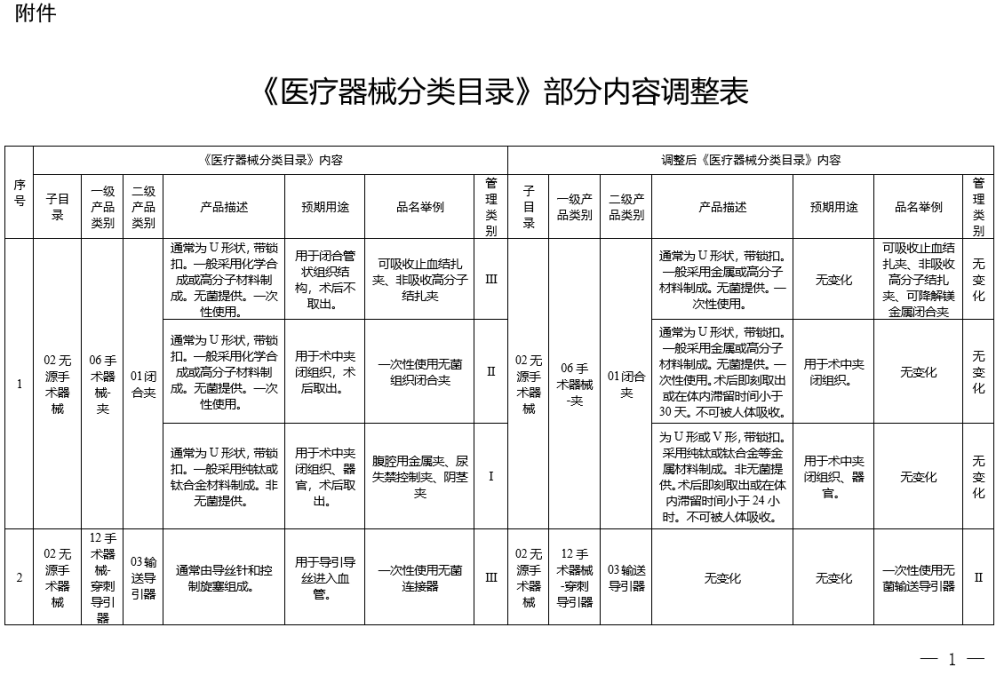
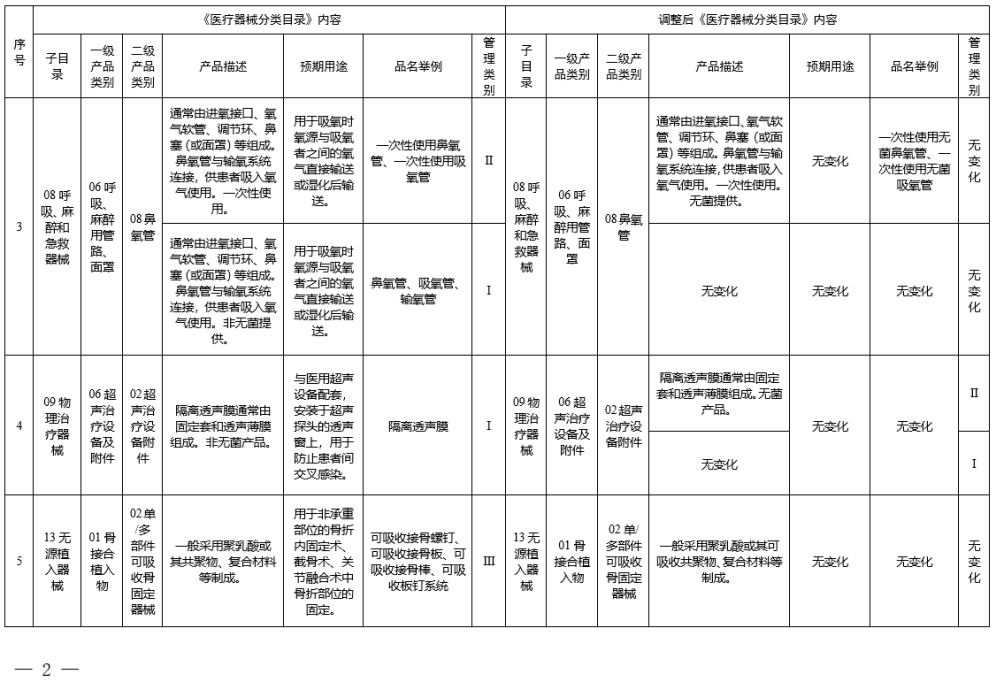
对31类医疗器械涉及《医疗器械分类目录》内容进行调整,具体调整内容见附件。
二、实施要求
(一)自本公告发布之日起,药品监督管理部门依据《医疗器械注册与备案管理办法》《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》《关于第一类医疗器械备案有关事项的公告》等,按照调整后的类别受理医疗器械注册申请或者办理备案。
对于已受理尚未完成注册审批(包括首次注册和延续注册)的医疗器械,药品监督管理部门继续按照原受理类别审评审批,准予注册的,核发医疗器械注册证,并在注册证备注栏注明调整后的产品管理类别。
对于已注册的医疗器械,其管理类别由第三类调整为第二类的,医疗器械注册证在有效期内继续有效。如需延续的,注册人应当在医疗器械注册证有效期届满6个月前,按照改变后的类别向相应药品监督管理部门申请延续注册,准予延续注册的,按照调整后的产品管理类别核发医疗器械注册证。
对于已注册的医疗器械,其管理类别由第二类调整为第一类的,医疗器械注册证在有效期内继续有效。注册证到期前,注册人应当向相应部门办理产品备案。
医疗器械注册证有效期内发生注册变更的,注册人应当向原注册部门申请变更注册。如原注册证为按照原《医疗器械分类目录》核发,本公告涉及产品的变更注册文件备注栏中应当注明公告实施后的产品管理类别。
(二)各级药品监督管理部门要加强《医疗器械分类目录》内容调整的宣贯培训,切实做好相关产品审评审批、备案和上市后监管工作。
来源:国家药监局
声明:文章为转载,其版权归原作者所有。转载仅用于分享,若涉及文章版权等问题,联系我方删除!
篇幅有限,查看全文请关注微信公众号“久顺集团技术服务”后查阅对应推文。
【久顺企管集团】医械注册的加速引擎!30年全球合规技术专家,中国\西班牙\荷兰\美国\英国均设公司,擅长产品注册全程辅导、技术文档编写、质量体系建立完善及咨询等服务,以及CE/FDA/UKCA/CFS等证书办理,具备优厚的咨询管理和技术服务经验及能力,护航产品全球范围高速畅行。








 沪公网安备 31011502005499
沪公网安备 31011502005499